Содержание ▲
- Строение вещества.
Модели строения газа,…
- Цель:
повторение основных понятий…
- Из истории…
Еще в Древней Греции, около 2,5…
- Основные положения МКТ
Молекулярно-кинетической…
- Атомы
Атомы очень малы. Их невозможно…
- Молекулы
Молекула - это мельчайшая частица…
- Молекулы
Молекулы состоят из атомов.
Размеры…
- Молекулы
У разных веществ молекулы могут…
- Строение вещества
Между молекулами в веществе…
-
Молекулярные силы
…
- Взаимодействие частиц вещества
Частицы веществ…
- Модели строения газов, жидкостей и…
- Строение твердых, жидких и газообразных…
- Слайд №14
- Рассмотрим задачи:
Подборка заданий по…
- ГИА-2009-7. В каком агрегатном состоянии…
- ГИА-2010-7. При охлаждении столбика спирта в…
- ГИА-2010-7. ρ1 — плотность вещества в жидком…
- Можно утверждать, что в сосуде после начала…
- ГИА-2010-26. Если тело находится внутри жидкости,…
- (ЕГЭ 2001 г., Демо) А16. В стакане с водой…
- (ЕГЭ 2005 г., ДЕМО) А8. Наименьшая…
- (ЕГЭ 2006 г., ДЕМО) А8. В жидкостях частицы…
- Литература
Агрегатные состояния вещества.…
- Скачать
- Похожие презентации
Слайды и текст этой презентации
Слайд 1

Описание слайда:
Строение вещества.
Модели строения газа, жидкости и
твердого тела
Подготовка к ГИА
Учитель: Попова И.А.
МОУ СОШ № 30 г. Белово
Белово 2010
Слайд 2

Описание слайда:
Цель:
повторение основных понятий молекулярно-кинетической теории, а также разбор задач различного уровня сложности в соответствии с кодификатором ГИА и планом демонстрационного варианта экзаменационной работы
Слайд 3

Описание слайда:
Из истории…
Еще в Древней Греции, около 2,5 тысяч лет назад, была выдвинута гипотеза о том, что вещество состоит из мельчайших частичек – атомов и молекул.
Основоположником идеи дискретного строения вещества считается древнегреческий философ Демокрит, живший около 470 года до новой эры. Демокрит считал, что все тела состоят из бесчисленного количества сверхмалых, невидимых глазу, неделимых частиц. "Они бесконечно разнообразны, имеют впадины и выпуклости, которыми сцепляются, образуя все материальные тела, а в природе существуют только атомы и пустота».
В научную теорию эта гипотеза превратилась только XVIII – XIX веках.
Если бы мы смогли рассмотреть окружающие нас тела через микроскоп, то увидели бы отдельные атомы и молекулы
Слайд 4
Описание слайда:
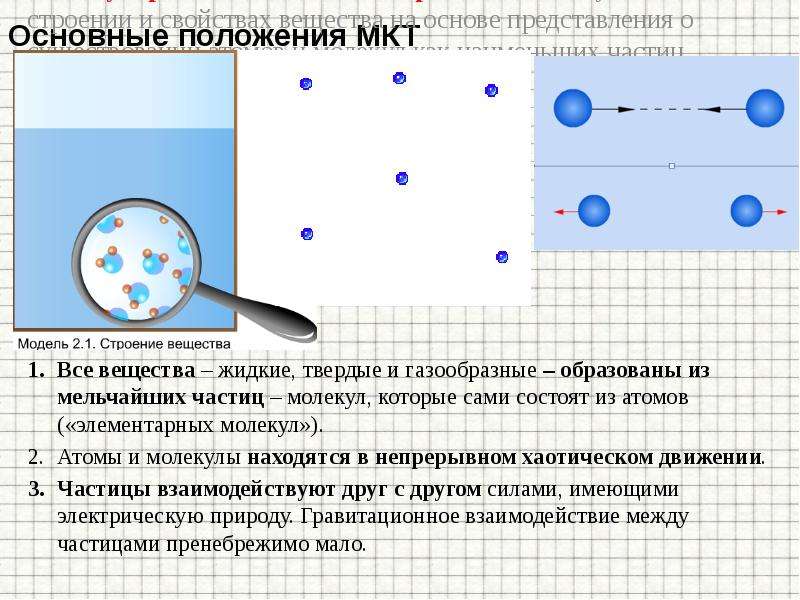
Основные положения МКТ
Молекулярно-кинетической теорией называют учение о строении и свойствах вещества на основе представления о существовании атомов и молекул как наименьших частиц химического вещества.
В основе молекулярно-кинетической теории лежат
три основных положения:
Слайд 5

Описание слайда:
Атомы
Атомы очень малы. Их невозможно разглядеть не только простым глазом, но и с помощью даже самого мощного оптического микроскопа.
В 1951 году Эрвин Мюллер изобрёл ионный микроскоп, позволивший в деталях разглядеть атомную структуру металла.
Атомы различных химических элементов отличаются друг от друга.
Слайд 6
Описание слайда:
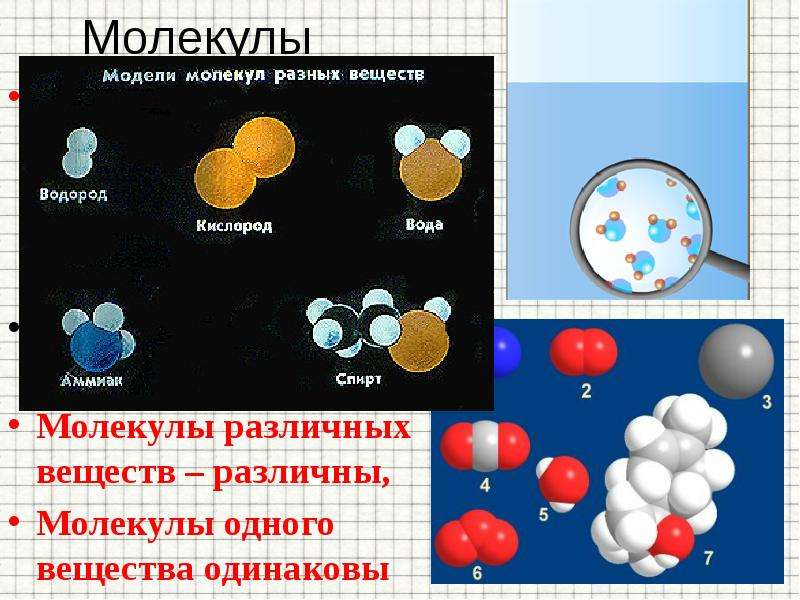
Молекулы
Молекула - это мельчайшая частица вещества, обладающая свойствами этого вещества.
Так, молекула сахара - сладкая, а соли – соленая.
Молекулы различных веществ – различны,
Молекулы одного вещества одинаковы
Слайд 7

Описание слайда:
Молекулы
Молекулы состоят из атомов.
Размеры молекул ничтожно малы.
Слайд 8
Описание слайда:
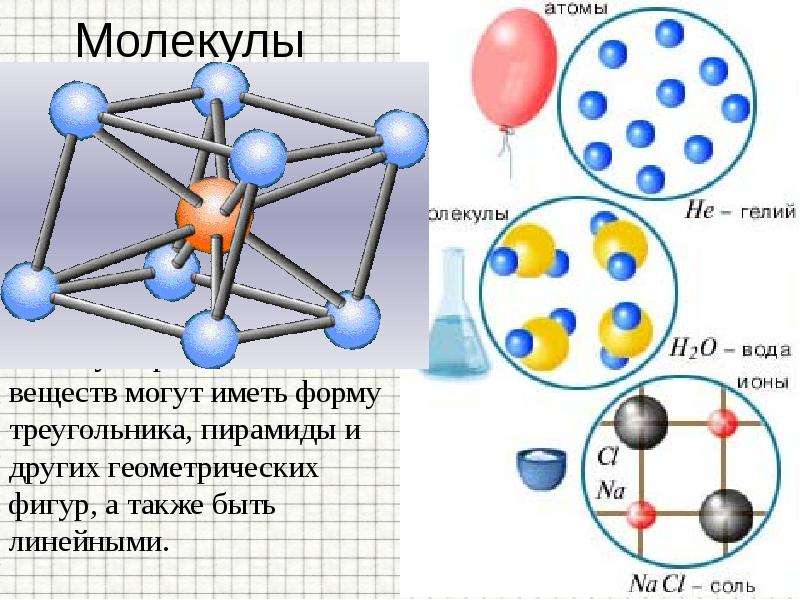
Молекулы
У разных веществ молекулы могут состоять из одного атома (инертные газы) или из нескольких одинаковых или различных атомов, или даже из сотен тысяч атомов (полимеры).
Молекулы различных веществ могут иметь форму треугольника, пирамиды и других геометрических фигур, а также быть линейными.
Слайд 9

Описание слайда:
Строение вещества
Между молекулами в веществе существуют промежутки.
Доказательствами существования промежутков служат изменение объема вещества, т.е. расширение и сжатие вещества при изменении температуры, и явление диффузии.
Слайд 10

Описание слайда:
Молекулярные силы
Слайд 11

Описание слайда:
Взаимодействие частиц вещества
Частицы веществ способны притягиваться друг к другу. Однако это притяжение возникает лишь тогда, когда поверхности тел очень гладкие (для этого и понадобилась зачистка лезвием) и, кроме того, плотно прижаты друг к другу.
Частицы веществ способны отталкиваться друг от друга. Это подтверждается тем, что жидкие, а особенно твердые тела очень трудно сжать.
Притяжение или отталкивание частиц веществ возникает лишь в том случае, если они находятся в непосредственной близости.
На расстояниях, чуть больших размеров самих частиц, они притягиваются.
На расстояниях, меньших размеров частиц, они отталкиваются.
Если же поверхности тел удалены на расстояние, заметно большее, чем размер частиц, то взаимодействие между ними не проявляется никак.
Слайд 12

Описание слайда:
Модели строения газов, жидкостей и твердых
Слайд 13

Описание слайда:
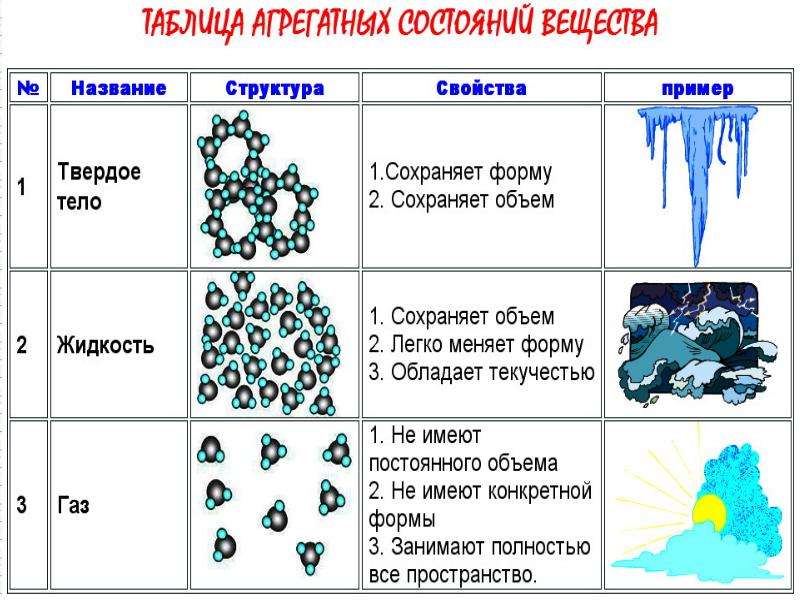
Строение твердых, жидких и газообразных тел
Большая часть вещества на Земле встречается в трех состояниях: твердом, жидком и газообразном. Часто эти состояния называют агрегатными.
В зависимости от условий одно и тоже вещество находится в каком-либо из них.
Например, лед, вода и водяной пар.
Или другой пример: воздух в вашей комнате — газ, но если его охладить до -193°C, он станет жидкостью, а если охладить до -213°C — твердым телом.
Слайд 14
Слайд 15

Описание слайда:
Рассмотрим задачи:
Подборка заданий по кинематике
(из заданий ГИА 2008-2010 гг.)
Слайд 16

Описание слайда:
ГИА-2009-7. В каком агрегатном состоянии находится на Земле вещество, если даже большая его масса имеет собственные форму и объем?
Слайд 17

Описание слайда:
ГИА-2010-7. При охлаждении столбика спирта в термометре
Слайд 18

Описание слайда:
ГИА-2010-7. ρ1 — плотность вещества в жидком состоянии, ρ2 — после кристаллизации. Какое соотношение плотностей справедливо?
Слайд 19

Описание слайда:
Можно утверждать, что в сосуде после начала нагревания при
неизменных условиях находятся
Слайд 20

Описание слайда:
ГИА-2010-26. Если тело находится внутри жидкости, плотность которой равна
плотности этого тела, то сила тяжести уравновешивается выталкивающей силой. Можно ли считать, что это тело находится в состоянии невесомости?
Слайд 21
Описание слайда:
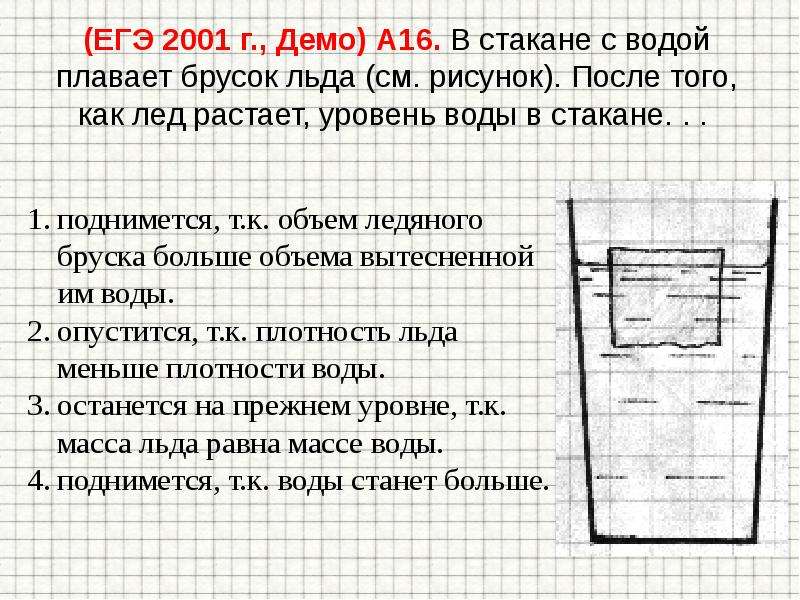
(ЕГЭ 2001 г., Демо) А16. В стакане с водой плавает брусок льда (см. рисунок). После того, как лед растает, уровень воды в стакане. . .
Слайд 22

Описание слайда:
(ЕГЭ 2005 г., ДЕМО) А8. Наименьшая упорядоченность в расположении частиц характерна для
Слайд 23

Описание слайда:
(ЕГЭ 2006 г., ДЕМО) А8. В жидкостях частицы совершают колебания возле положения равновесия, сталкиваясь с соседними частицами. Время от времени частица совершает «прыжок» к другому положению равновесия. Какое свойство жидкостей можно объяснить таким характером движения частиц?
малую сжимаемость
текучесть
давление на дно сосуда
изменение объема при нагревании
Слайд 24
![Литература
Агрегатные состояния вещества. Аргументы и факты //[Электронный ресурс]// http://gazeta.aif.ru/online/kids/106/de02_01
Гутник, Е. М., Физика. 7 класс. Учебник для общеобразовательных школ / Е. М. Гутник, А. В. Перышкин. - М.: Дрофа, 2009. – 302 с.
Зорин, Н.И. ГИА 2010. Физика. Тренировочные задания: 9 класс / Н.И. Зорин. – М.: Эксмо, 2010. – 112 с. – (Государственная (итоговая) аттестация (в новой форме).
Кабардин, О.Ф. Физика. 9 кл.: сборник тестовых заданий для подготовки к итоговой аттестации за курс основной школы / О.Ф. Кабардин. – М.: Дрофа, 2008. – 219 с;
Молекулярные силы. Единая коллекция цифровых образовательных ресурсов //[Электронный ресурс]// http://collection.edu.yar.ru/catalog/res/04d94d50-42fb-4b56-8912-96f08359c717/view/
Основные положения теории. Портал Естественных Наук//[Электронный ресурс]// http://e-science.ru/physics/theory/?t=224
Перышкин, А. В., Физика. 7 класс. Учебник для общеобразовательных школ / А. В. Перышкин. - М.: Дрофа, 2009. – 198 с.
Перышкин, А. В., Физика. 8 класс. Учебник для общеобразовательных школ / А. В. Перышкин. - М.: Дрофа, 2009. – 196 с.
Сила упругости. Закон Гука. Весь курс Физики //[Электронный ресурс]// http://fizika.ayp.ru/1/1_12.html
Тема 8. Молекулярно-кинетическая теория. Dproc.do.am //[Электронный ресурс] // http://dproc.do.am/publ/3-1-0-12
Федеральный институт педагогических измерений. Контрольные измерительные материалы (КИМ) Физика ГИА-9 2010 г. //[Электронный ресурс]// http://fipi.ru/view/sections/214/docs/
Федеральный институт педагогических измерений. Контрольные измерительные материалы (КИМ) Физика ЕГЭ 2001-2010 //[Электронный ресурс]// http://fipi.ru/view/sections/92/docs/](/documents_2/5855b1b9ee3378e5d18285be383d4fe4/img23.jpg)
Описание слайда:
Литература
Агрегатные состояния вещества. Аргументы и факты //[Электронный ресурс]// http://gazeta.aif.ru/online/kids/106/de02_01
Гутник, Е. М., Физика. 7 класс. Учебник для общеобразовательных школ / Е. М. Гутник, А. В. Перышкин. - М.: Дрофа, 2009. – 302 с.
Зорин, Н.И. ГИА 2010. Физика. Тренировочные задания: 9 класс / Н.И. Зорин. – М.: Эксмо, 2010. – 112 с. – (Государственная (итоговая) аттестация (в новой форме).
Кабардин, О.Ф. Физика. 9 кл.: сборник тестовых заданий для подготовки к итоговой аттестации за курс основной школы / О.Ф. Кабардин. – М.: Дрофа, 2008. – 219 с;
Молекулярные силы. Единая коллекция цифровых образовательных ресурсов //[Электронный ресурс]// http://collection.edu.yar.ru/catalog/res/04d94d50-42fb-4b56-8912-96f08359c717/view/
Основные положения теории. Портал Естественных Наук//[Электронный ресурс]// http://e-science.ru/physics/theory/?t=224
Перышкин, А. В., Физика. 7 класс. Учебник для общеобразовательных школ / А. В. Перышкин. - М.: Дрофа, 2009. – 198 с.
Перышкин, А. В., Физика. 8 класс. Учебник для общеобразовательных школ / А. В. Перышкин. - М.: Дрофа, 2009. – 196 с.
Сила упругости. Закон Гука. Весь курс Физики //[Электронный ресурс]// http://fizika.ayp.ru/1/1_12.html
Тема 8. Молекулярно-кинетическая теория. Dproc.do.am //[Электронный ресурс] // http://dproc.do.am/publ/3-1-0-12
Федеральный институт педагогических измерений. Контрольные измерительные материалы (КИМ) Физика ГИА-9 2010 г. //[Электронный ресурс]// http://fipi.ru/view/sections/214/docs/
Федеральный институт педагогических измерений. Контрольные измерительные материалы (КИМ) Физика ЕГЭ 2001-2010 //[Электронный ресурс]// http://fipi.ru/view/sections/92/docs/
Презентацию на
тему Модели строения газа, жидкости и твердого тела можно скачать бесплатно ниже: