Слайды и текст этой презентации
Слайд 1
Описание слайда:
Щелочные и щелочно-земельные металлы
Na K Li
Cs Ba
Rb Fr
Sr
Ca
Слайд 2

Описание слайда:
Щелочные металлы – элементы IA группы
Перечислите известные вам щелочные металлы.
Сколько электронов на внешнем энергетическом уровне у атомов всех щелочных металлов?
Восстановителями или окислителями являются щелочные металлы.
Что имеют в виду говоря о металлических свойствах элемента?
Слайд 3

Описание слайда:
Из истории открытия элементов
19 ноября 1907 года в Лондоне на заседании Королевского химического общества сэр Хемфри Деви объявил об открытии им новых элементов –натрия и калия.
На протяжении 17 лет эти элементы не находили применения, их называли «элементами только для химиков».
Слайд 4

Слайд 5

Описание слайда:
3 января 1959 года
В небе появилась комета. Необычная комета – искусственная: из летящей к Луне советской космической ракеты было выпущено облако паров натрия. Пурпурное свечение этих паров позволило уточнить траекторию первого летательного аппарата, прошедшего по маршруту Земля-Луна.
Слайд 6

Описание слайда:
Физические свойства
Какое строение характерно для кристаллов щелочных металлов?
Как изменяются температуры кипения и плавления?
Какой самый легкий из щелочных металлов?
Слайд 7
Описание слайда:
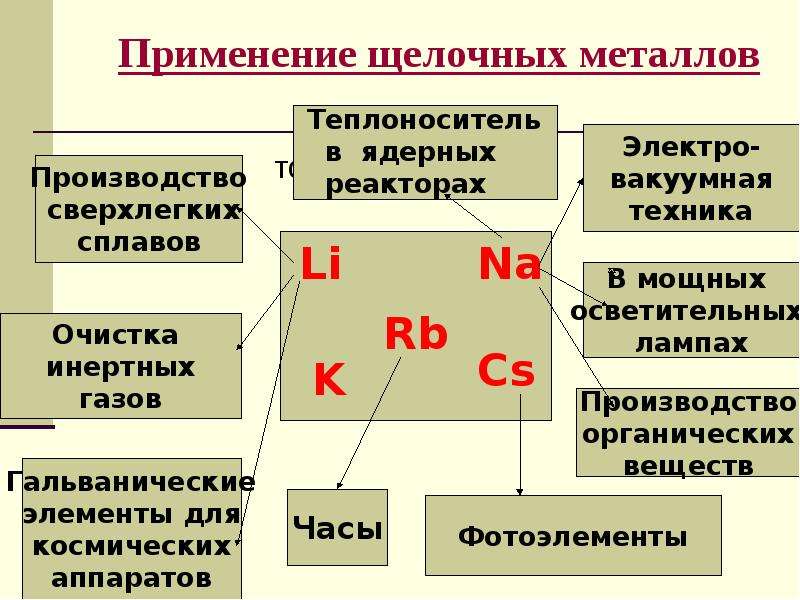
Применение щелочных металлов
тото
Слайд 8

Описание слайда:
Соединения щелочных металлов
В ветхом завете упоминается некое вещество «нетер». Это вещество употребляли как моющее средство. Скорее всего оно образовалось в соленых египетских озерах с известковыми берегами. Об этом веществе, но под названием «нитрон» писали позже греческие авторы –Аристотель, Диоскорид.
Как вы думаете, о каком веществе идет речь?
Слайд 9
Описание слайда:
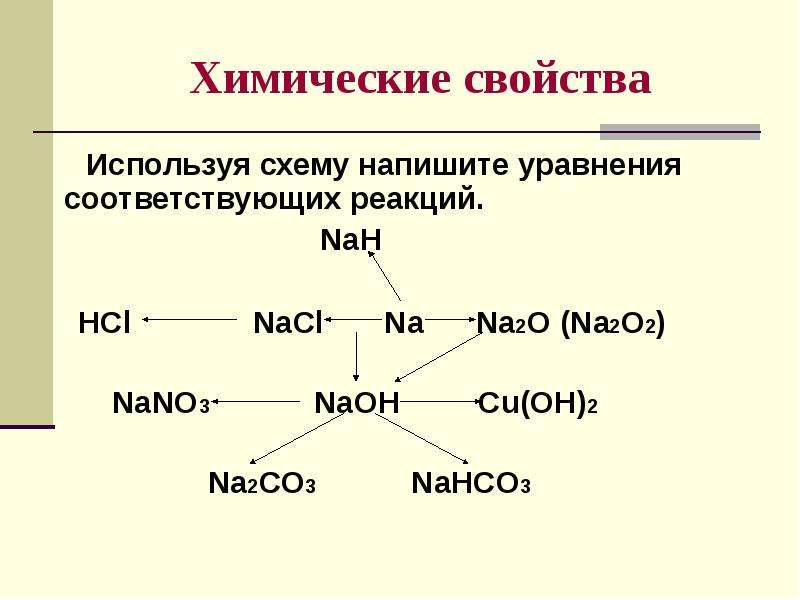
Химические свойства
Используя схему напишите уравнения соответствующих реакций.
NaH
HCl NaCl Na Na2O (Na2O2)
NaNO3 NaOH Cu(OH)2
Na2CO3 NaHCO3
Слайд 10

Описание слайда:
Щелочноземельные металлы-элементы IIA группы
Щелочноземельными являются не все элементы IIА группы, а только начиная с кальция и вниз по группе.
Оксиды этих элементов («земли» - по старинной терминологии) взаимодействуют с водой, образуя щелочи.
Напишите уравнения реакции любого из оксидов металлов с водой.
Слайд 11
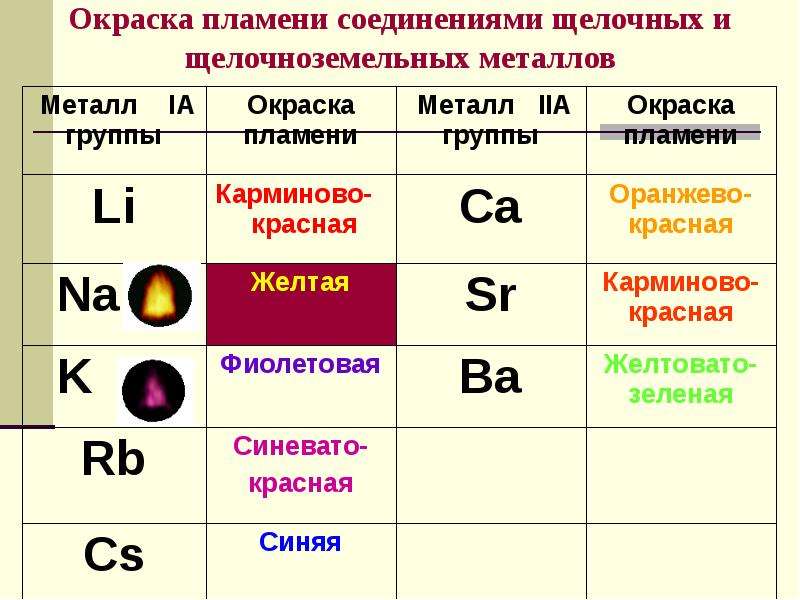
Описание слайда:
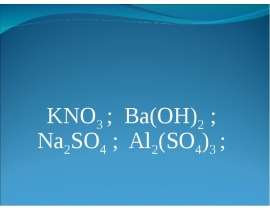
Окраска пламени соединениями щелочных и щелочноземельных металлов
Слайд 12

Описание слайда:
Кальций –типичный представитель щелочноземельных металлов
Дайте названия соединениям кальция:
CaO
Ca(OH)2
CaCO3
CaHCO3
Вспомните тривиальные названия этих веществ
Слайд 13
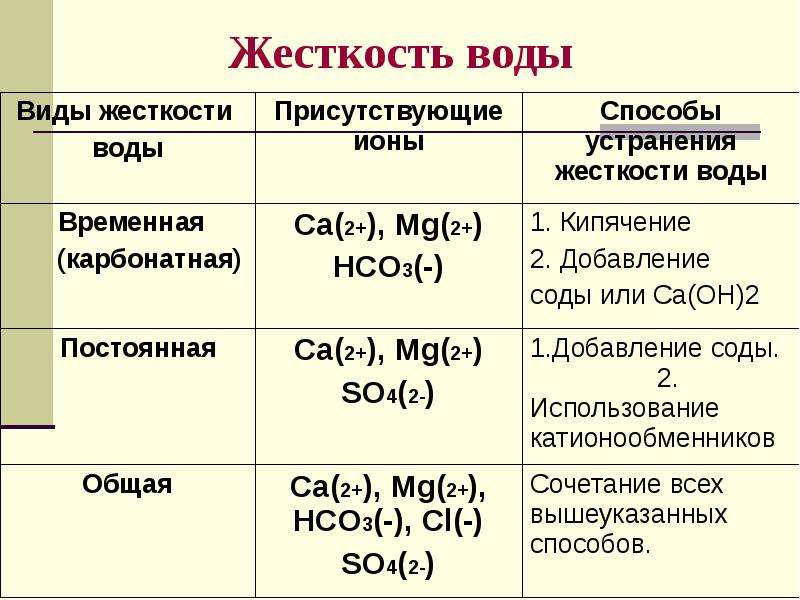
Описание слайда:
Жесткость воды
Слайд 14
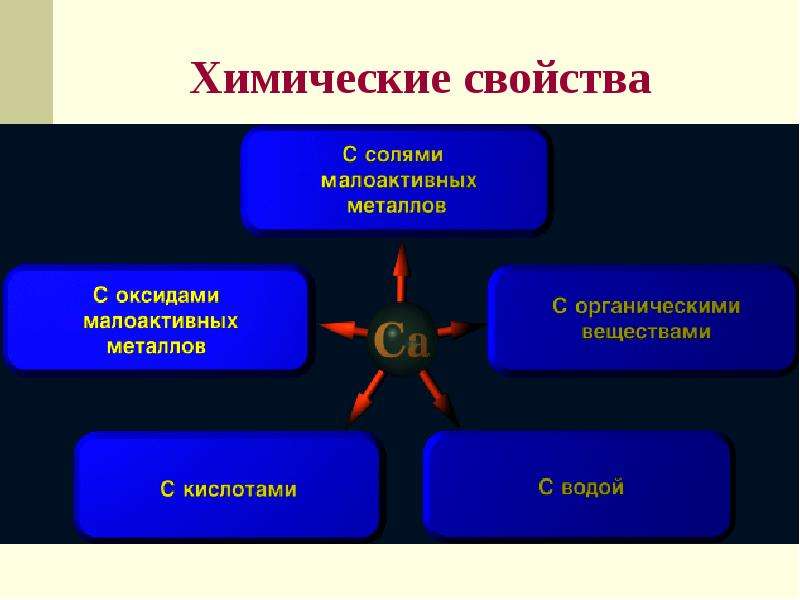
Описание слайда:
Химические свойства
Слайд 15
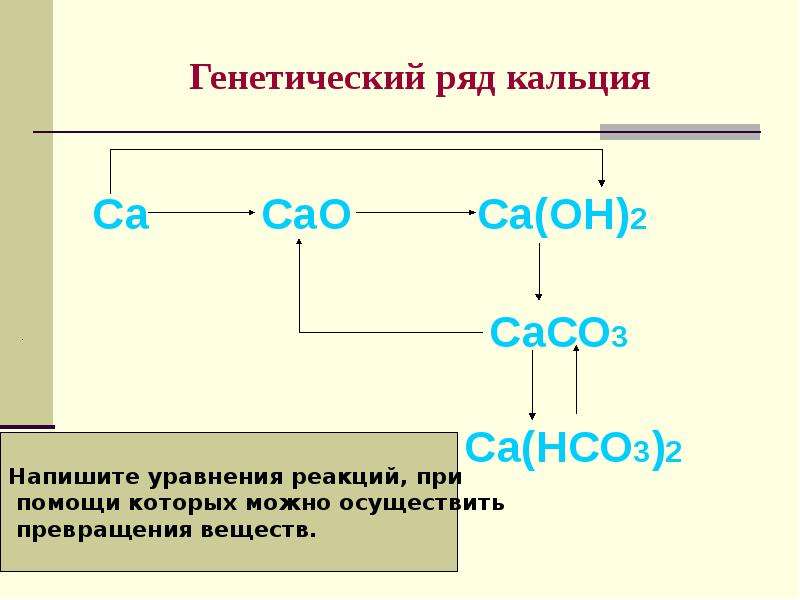
Описание слайда:
Генетический ряд кальция
Са СаО Са(ОН)2
СаСО3
Са(НСО3)2
Слайд 16

Описание слайда:
Кальций в природе
Кальциевые горные породы – известняк, мрамор, мел.
Слайд 17

Описание слайда:
Мел, известняк, мрамор не растворяются в чистой воде, но растворимы в кислых растворах, даже таких слабых, как природная вода.
При просачивании воды с поверхности земли через залежи
известняка происходят
процессы:
Если порода залегает под тонким слоем почвы – образуются провалы;
Слайд 18

Описание слайда:
Как называются отложения, свисающие в виде гигантских сосулек со свода пещеры? А растущие навстречу им со дна пещеры колонны?
Слайд 19

Описание слайда:
При воздействии
кислотных дождей
строения разрушаются.
Слайд 20

Описание слайда:
? ? ?
Каково значение щелочных и щелочно-земельных металлов в жизни человека?
Как изменяются свойства оксидов и гидроксидов в группах при
увеличении заряда ядра?
Какой из элементов калий
или цезий является более
сильным восстановителем?
Слайд 21

Описание слайда:
Спасибо за работу!
Презентацию на
тему Щелочные и щелочноземельные металлы можно скачать бесплатно ниже: