Описание слайда:
А знаете ли вы, что …
… разведя 1 мл чернил в 1 литре воды, а затем 1 мл этого раствора – в еще одном литре воды, мы получим разбавление в миллион раз. Несмотря на это, получившийся раствор будет иметь вполне заметную окраску. Отсюда следует, что объем частичек чернил намного меньше, чем миллионная часть миллилитра!
… сохранилось описание одного исторического опыта, в котором в свинцовый шар налили воду и прочно его запаяли. По шару ударили молотом, надеясь, что он сплющится и сожмет воду. И что же? Шар сплющился, но вода не сжалась, она просочилась сквозь стенки шара. Молекулы воды были продавлены через промежутки между частицами свинца.
… молекулы воздуха в твоей комнате мчатся со скоростью примерно полкилометра в секунду. Это составляет около 2000 км/ч – быстрее звука! Только имей в виду, что эта скорость средняя, ведь скорости всех молекул неодинаковы.
… диффузия веществ – очень распространенное явление. Диффузия происходит при засолке овощей, копчении рыбы, поступлении питательных веществ из желудка в кровь, всасывании влаги корнями растений, проникновении сахара внутрь ягод в вареньях и др.
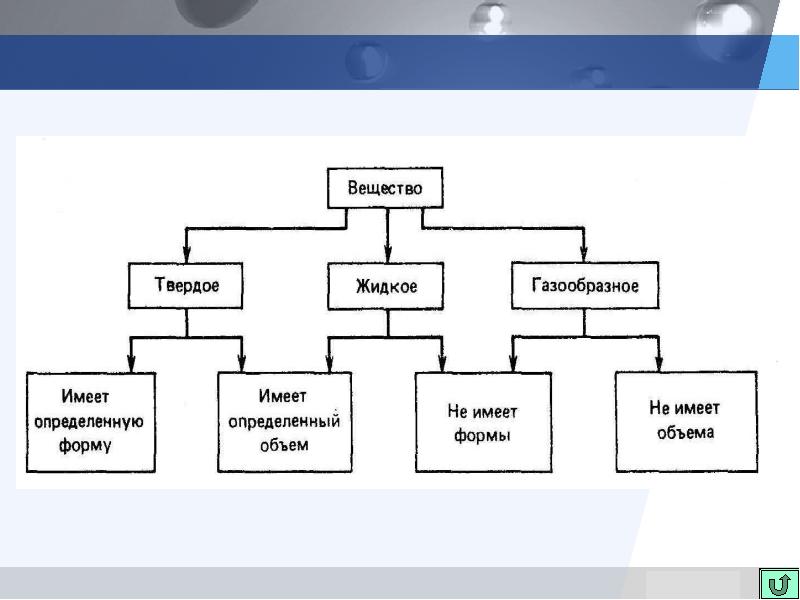
… оконные стекла в зданиях прошлого века в нижней части заметно толще, чем в верхней. Так происходит потому, что стекло, как и всякое аморфное тело, обладает текучестью.
… кристаллические тела тоже могут обладать текучестью. Например, горные ледники медленно стекают в долины. Текучесть кристаллов объясняется дефектами их кристаллической решетки.
… чтобы метровый столб воды или спирта сжать на 1 см, нужно большое давление – около 200 атмосфер. Но чтобы также сжать стержень из металла, нужно давление уже в 10 тысяч атмосфер!
… установлено, что молекулы воды совершают около 100 миллиардов перескоков в секунду.
… слово "газ" придумано учеными. Оно произведено от греческого слова "хаос" – беспорядок.
… литр воздуха можно сжать до объема наперстка.
… каждая молекула воздуха испытывает ни много, ни мало – четыре миллиарда столкновений в секунду со своими "соседками".
… с поверхности всех водоемов на Земле ежесуточно испаряется около 7000 км3 воды. Бассейн с таким количеством воды имел бы размеры 80 х 90 км при километре глубины!