Слайды и текст этой презентации
Слайд 1

Описание слайда:
Тема урока: «Законы
электролиза»
Слайд 2

Описание слайда:
Задачи урока:
1. Обучающие: обеспечить усвоение предметного содержания темы «Законы электролиза»:
- на первом уровне отличать электролиты от других видов веществ по электропроводности;
- на втором уровне формировать понятие электролитов и их практического применения;
- на третьем уровне сравнивать, анализировать, формировать их физические свойства;
- на четвертом уровне оперировать понятиями темы, применять практические знания для объяснения закона Фарадея;
- на пятом уровне осознанно использовать полученные знания.
Слайд 3

Описание слайда:
Задачи урока:
2. Развивающая. Развитие основных способов мыслительной деятельности (сравнение, сопоставление, анализ, обобщение). Развивать память, познавательные интересы, самостоятельность в организации труда с персональным компьютером. Оценить результаты своей работы.
Слайд 4

Описание слайда:
Задачи урока:
3. Воспитательная. Способствовать формированию коммуникативных качеств, трудолюбия, ответственности за порученное дело.
Слайд 5

Описание слайда:
Методическая цель.
Показать эффективность использования элементов технологии критического мышления.
Слайд 6

Описание слайда:
Тип урока
Комбинированный урок (использование элементов технологии критического мышления)
Слайд 7

Описание слайда:
Изучать, открывать, удивлять,
Верить в силу наук для людей
И природы закон применять,
Как его применял Фарадей.
Слайд 8

Описание слайда:
Фаза вызова
Слайд 9
Описание слайда:
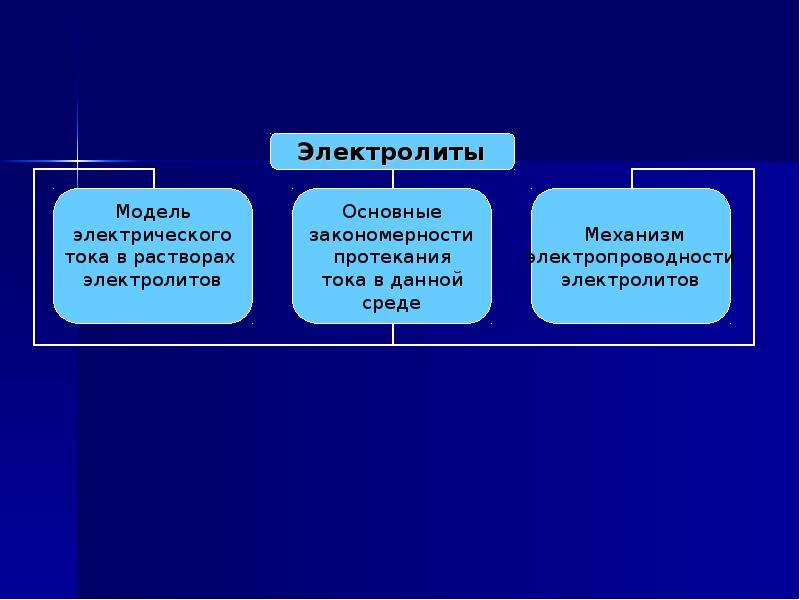
Вспомним, что мы знаем об электролитах.
Для этого заполним кластер.
Слайд 10
Слайд 11
Слайд 12
Слайд 13

Описание слайда:
Проверим ваши знания.
Для этого проведем
физический диктант
Слайд 14

Описание слайда:
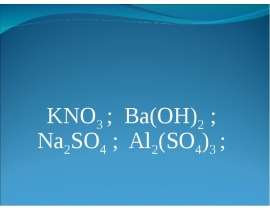
Электролиты – это
Электролиты – это
Слайд 15

Описание слайда:
Ответ правильный.
Вы получаете 1 балл.
Слайд 16

Описание слайда:
Ответ неправильный.
Ответ неправильный.
Правильный ответ:
Электролиты – это растворы неорганических солей, кислот, щелочей.
Вы получаете 0 баллов.
Слайд 17

Слайд 18

Описание слайда:
Ответ правильный.
Вы получаете 1 балл.
Слайд 19

Описание слайда:
Ответ неправильный.
Ответ неправильный.
Правильный ответ:
Носителями зарядов в электролитах являются положительные и отрицательные ионы, которые образуются вследствие электролитической диссоциации.
Вы получаете 0 баллов.
Слайд 20

Слайд 21

Описание слайда:
Ответ правильный.
Вы получаете 1 балл.
Слайд 22

Описание слайда:
Ответ неправильный.
Ответ неправильный.
Правильный ответ:
Электролитическая диссоциация - это распад молекул электролитов на ионы.
Вы получаете 0 баллов.
Слайд 23

Слайд 24

Описание слайда:
Ответ правильный.
Вы получаете 1 балл.
Слайд 25

Описание слайда:
Ответ неправильный.
Ответ неправильный.
Правильный ответ:
Рекомбинация - это процесс, противоположный диссоциации.
Вы получаете 0 баллов.
Слайд 26

Слайд 27

Описание слайда:
Ответ правильный.
Вы получаете 1 балл.
Слайд 28

Описание слайда:
Ответ неправильный.
Ответ неправильный.
Правильный ответ:
Электролиз - это окислительно-восстановительная реакция, протекающая на электродах при прохождении электрического тока через электролит.
Вы получаете 0 баллов.
Слайд 29

Слайд 30

Описание слайда:
Ответ правильный.
Вы получаете 1 балл.
Слайд 31

Описание слайда:
Ответ неправильный.
Ответ неправильный.
Правильный ответ:
Окислительно-восстановительная реакция - это реакция с изменением степени окисления элементов.
Вы получаете 0 баллов.
Слайд 32

Слайд 33

Описание слайда:
Ответ правильный.
Вы получаете 1 балл.
Слайд 34

Описание слайда:
Ответ неправильный.
Ответ неправильный.
Правильный ответ:
Проводимость электролитов называют ионной.
Вы получаете 0 баллов.
Слайд 35

Слайд 36

Описание слайда:
Ответ правильный.
Вы получаете 1 балл.
Слайд 37

Описание слайда:
Ответ неправильный.
Ответ неправильный.
Правильный ответ:
Катод – это электрод, соединенный с отрицательным полюсом источника тока.
Вы получаете 0 баллов.
Слайд 38

Слайд 39

Описание слайда:
Ответ правильный.
Вы получаете 1 балл.
Слайд 40

Описание слайда:
Ответ неправильный.
Ответ неправильный.
Правильный ответ:
Анод – это электрод, соединенный с положительным полюсом источника тока.
Вы получаете 0 баллов.
Слайд 41

Слайд 42

Описание слайда:
Ответ правильный.
Вы получаете 1 балл.
Слайд 43

Описание слайда:
Ответ неправильный.
Ответ неправильный.
Правильный ответ:
Электролиз применяют для получения металлов (меди, алюминия) электролитическим способом, в гальванопластике и др.
Вы получаете 0 баллов.
Слайд 44

Описание слайда:
Посчитайте свои баллы и сообщите учителю.
Слайд 45

Описание слайда:
Итог по фазе вызова.
«Фишбон»
Слайд 46

Описание слайда:
Фаза осмысления
Продолжаем нашу работу.
Следующая фаза осмысления.
Попробуем установить основные закономерности протекания электрического тока в растворах электролитов.
Слайд 47

Описание слайда:
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 48

Описание слайда:
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 49

Описание слайда:
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 50

Описание слайда:
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 51

Описание слайда:
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 52
Описание слайда:
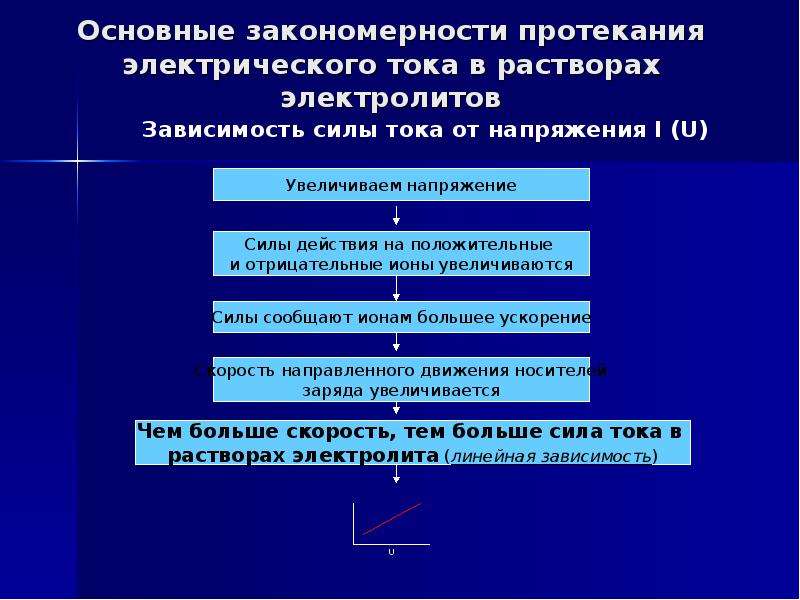
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 53

Описание слайда:
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 54
Описание слайда:
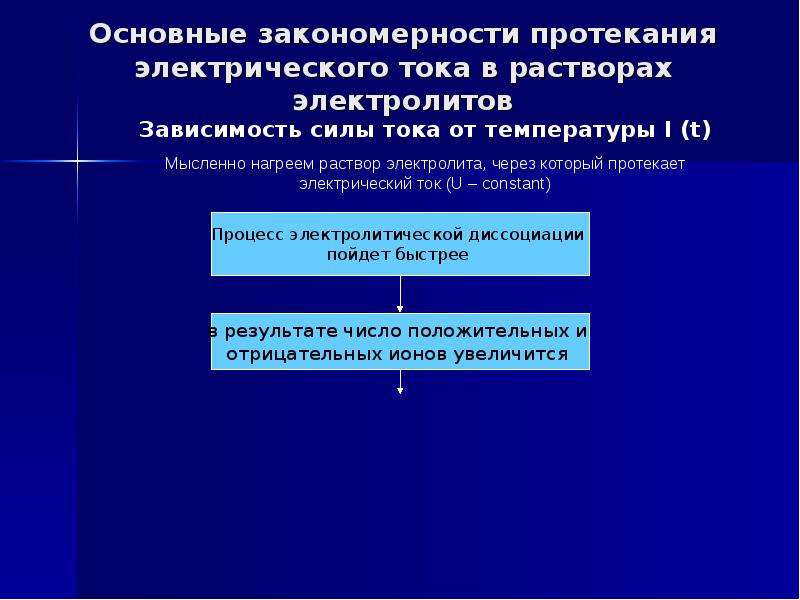
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 55
Описание слайда:
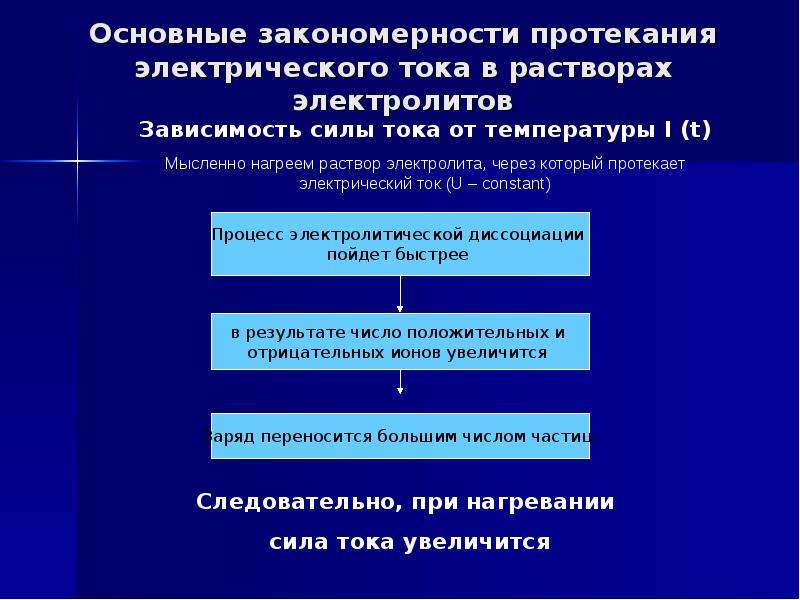
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 56

Описание слайда:
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 57

Описание слайда:
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 58

Описание слайда:
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 59

Описание слайда:
Повторим основные закономерности протекания электрического тока в растворах электролитов.
Повторим основные закономерности протекания электрического тока в растворах электролитов.
Слайд 60
Описание слайда:
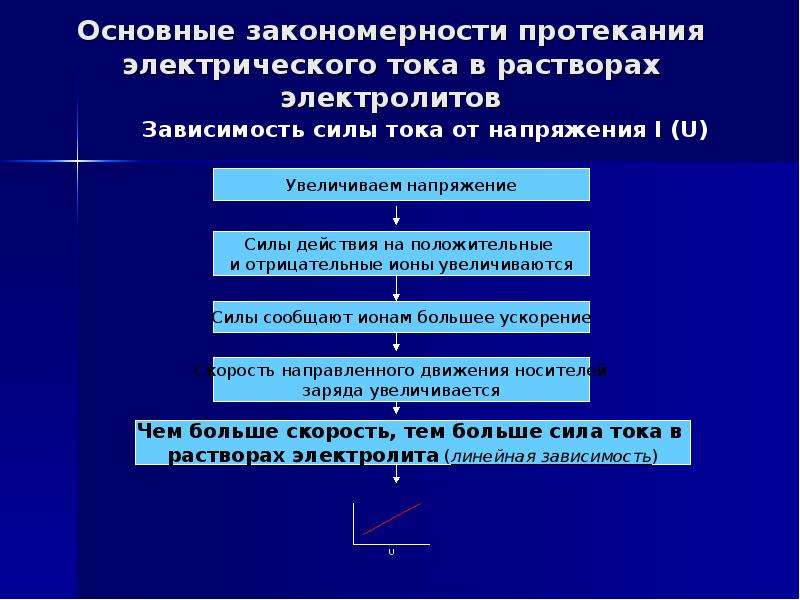
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 61
Описание слайда:
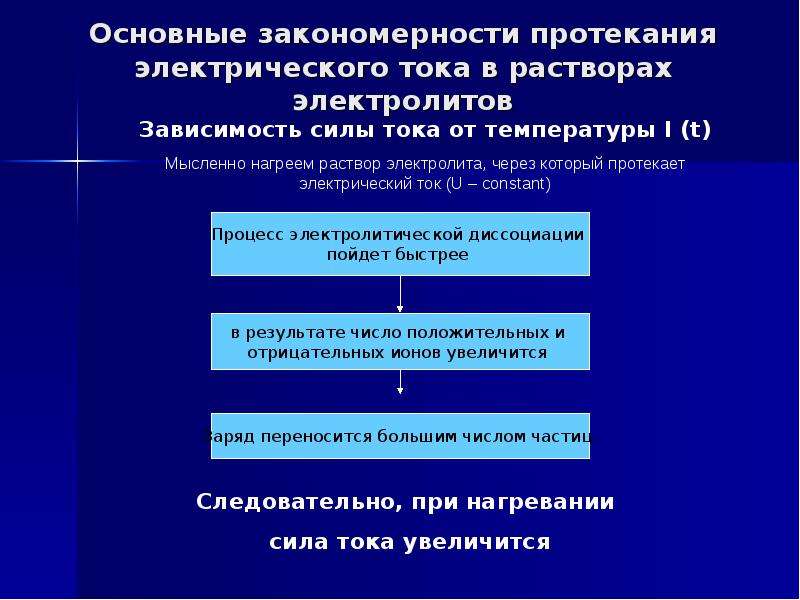
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 62

Описание слайда:
Основные закономерности протекания электрического тока в растворах электролитов
Слайд 63
Описание слайда:
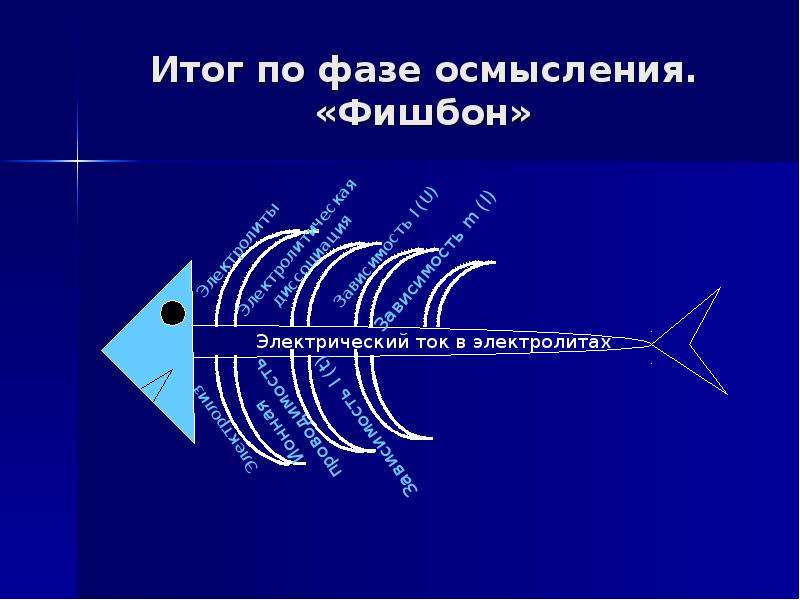
Итог по фазе осмысления.
«Фишбон»
Слайд 64

Описание слайда:
Фаза осмысления
(продолжение)
Зная механизм проводимости электролитов можно определить массу вещества, выделившегося при электролизе. Чтобы решить эту задачу, необходимо получить и изучить законы Фарадея.
Слайд 65

Описание слайда:
Самостоятельная работа с учебником
I закон Фарадея.
Алгоритм.
Слайд 66

Описание слайда:
1. Запишите формулу массы вещества
Слайд 67

Описание слайда:
2. Свяжите массу атома с молярной массой.
Слайд 68

Описание слайда:
3. Находим N – число ионов, проходящих через раствор электролитов.
а) Каждый одновалентный ион несет заряд, равный заряду электрона e. Если валентность равна n, кратный ему заряд равен ne.
Слайд 69

Описание слайда:
3. Находим N – число ионов, проходящих через раствор электролитов.
г) так как в выражении (2) правой части все физические величины, кроме q, постоянны, формулу (2) записываем
Слайд 70

Описание слайда:
4. Электрохимический эквивалент
Слайд 71

Описание слайда:
Самостоятельная работа с учебником
II закон Фарадея.
Алгоритм.
Слайд 72

Описание слайда:
1. Дайте определение химического эквивалента.
Химический эквивалент - это отношение атомной (А) массы вещества к его валентности (n)
Слайд 73

Описание слайда:
2. Запишите второй закон Фарадея.
Второй закон Фарадея: электрохимический эквивалент пропорционален химическому эквиваленту данного вещества.
Слайд 74

Описание слайда:
3. Дайте определение постоянной Фарадея.
Постоянная Фарадея F – численно равна заряду, который должен пройти через электролит для выделения на электроде количества вещества, равного его химическому эквиваленту.
Слайд 75
Описание слайда:
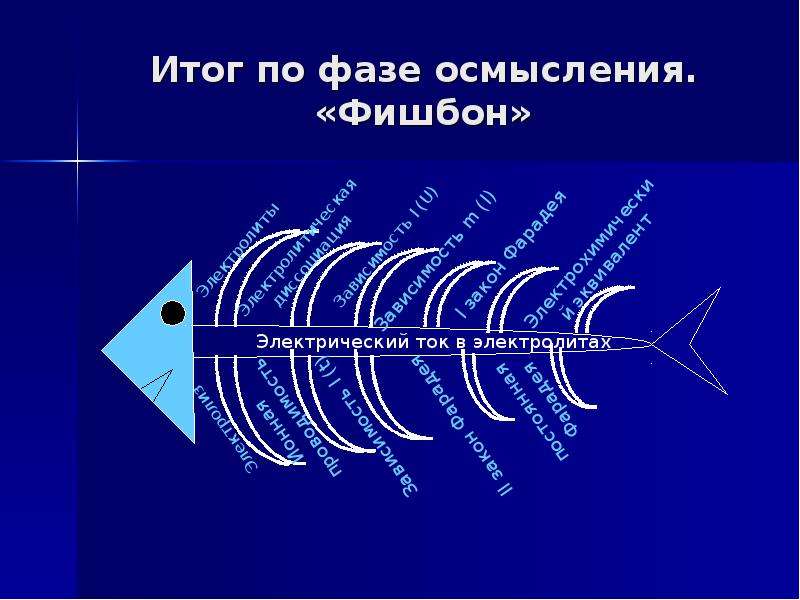
Итог по фазе осмысления.
«Фишбон»
Слайд 76

Описание слайда:
Фаза практического осмысления
(работа с дополнительной литературой)
Законы Фарадея нашли практическое применение в науке и технике, в частности для определения заряда одновалентного иона.
Слайд 77

Описание слайда:
Мозговая атака
(мысли по кругу)
Как решать задачи, используя законы электролиза (памятка).
Слайд 78

Описание слайда:
Мозговая атака
(мысли по кругу)
Последовательность решения задач.
Слайд 79

Описание слайда:
Фаза практического осмысления
(работа с дополнительной литературой)
Применение законов Фарадея при решении качественных и количественных задач.
Слайд 80
Описание слайда:
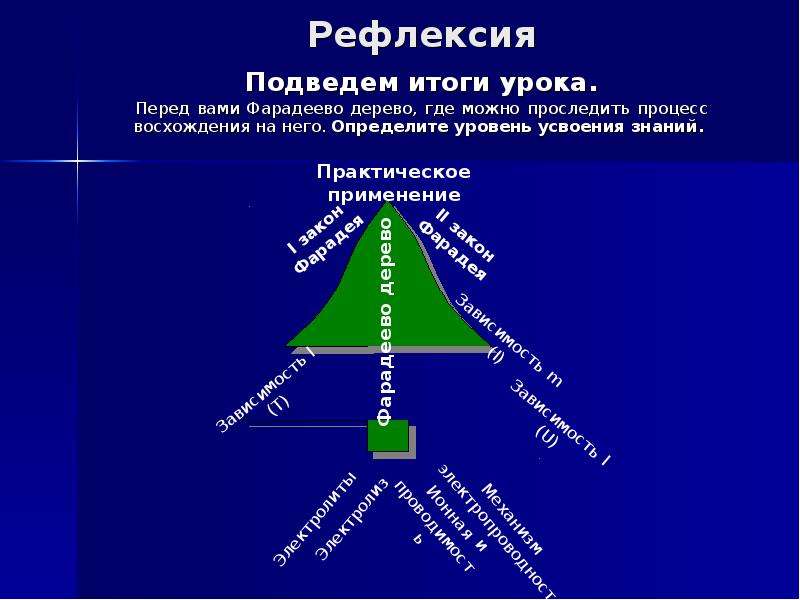
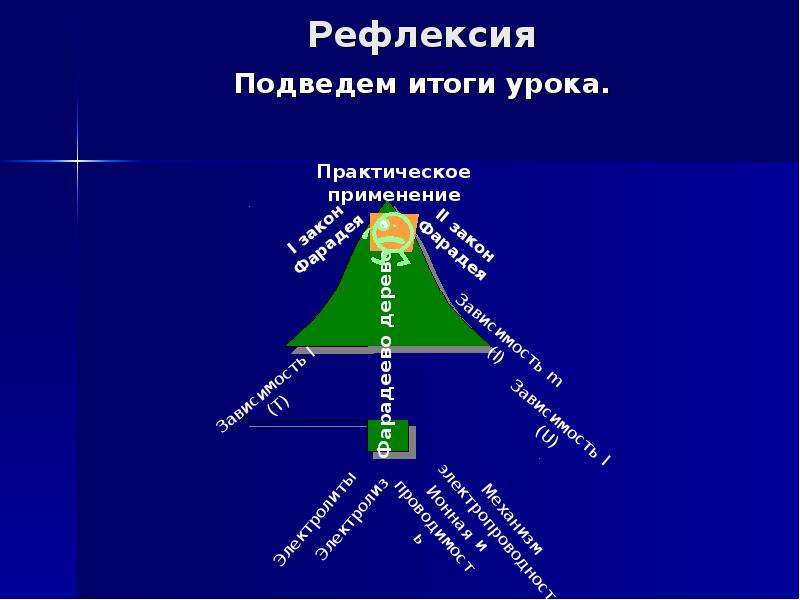
Рефлексия
Подведем итоги урока.
Перед вами Фарадеево дерево, где можно проследить процесс восхождения на него. Определите уровень усвоения знаний.
Слайд 81
Описание слайда:
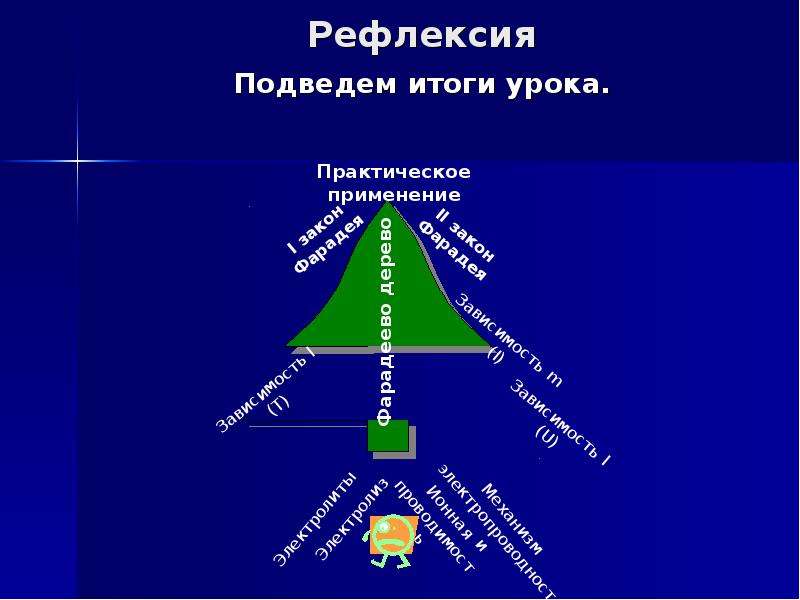
Рефлексия
Подведем итоги урока.
Слайд 82
Описание слайда:
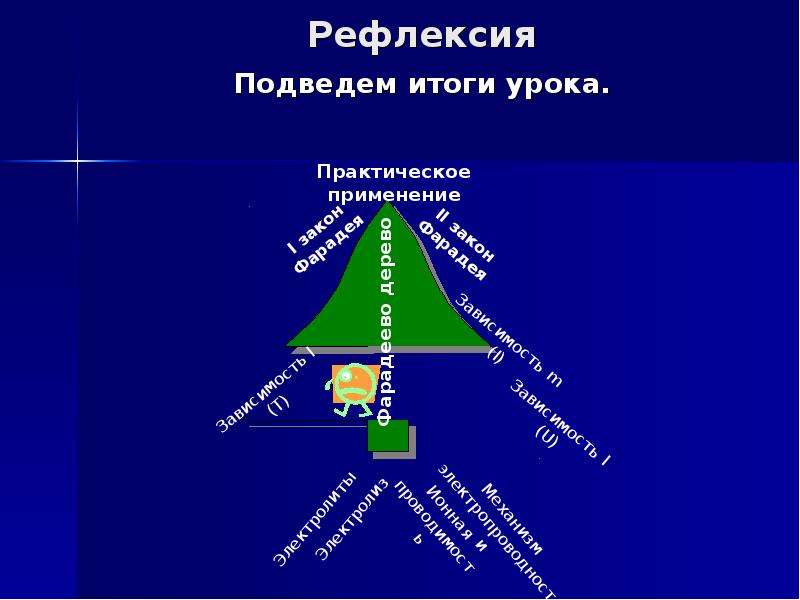
Рефлексия
Подведем итоги урока.
Слайд 83
Описание слайда:
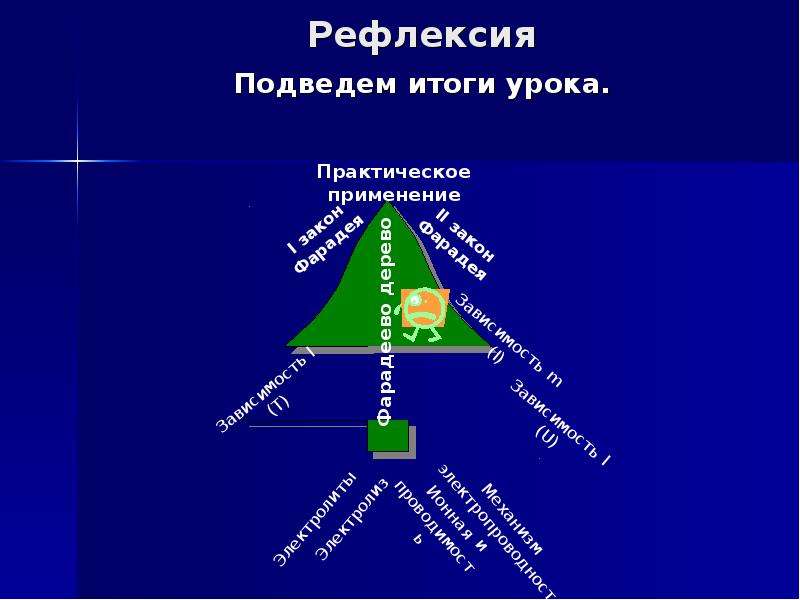
Рефлексия
Подведем итоги урока.
Слайд 84
Описание слайда:
Рефлексия
Подведем итоги урока.
Слайд 85
Описание слайда:
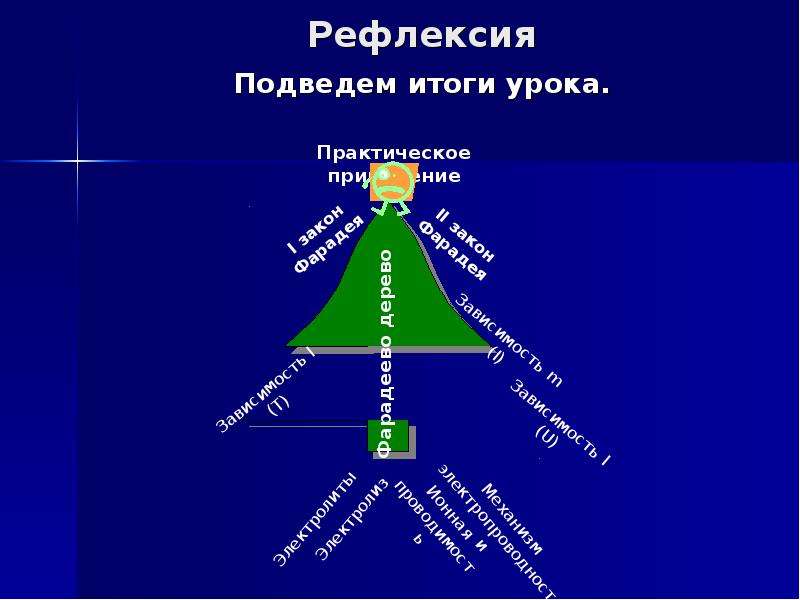
Рефлексия
Подведем итоги урока.
Презентацию на
тему Законы электролиза можно скачать бесплатно ниже: