Описание слайда:
Відкриття електрона : Якщо відволіктися від того, що передувало відкриттю першої елементарної частки - електрона, і від того, що супроводжувало цієї визначної події, можна сказати коротко: в 1897 році відомий англійський фізик Томсон Джозеф Джон(1856-1940 рр.) Виміряв питому заряду q/m катодно-променевих частинок - "корпускул",як він їх назвав, по відхиленню катодних променів *) в електричному та магнітному полях . З зіставлення отриманого числа з відомим на той час питомим зарядом одновалентного іона водню, шляхом непрямих міркувань він прийшов до висновку,що маса цих часток, які отримали пізніше назву "електрони",значно менша (більш ніж у тисячу разів) маси самого легкого іона водню. У тому ж,1897 році він висунув гіпотезу, що електрони є складовою частиною атомів,а катодні промені - не атоми чи не електромагнітне випромінювання, як вважали деякі дослідники властивостей променів. Томсон писав: "Таким чином,катодні промені являють собою новий стан речовини, істотно відмінне від звичайного газоподібного стану ...; в цьому новому стані матерія являє собою речовину, з якої побудовані всі елементи ". З 1897 року корпускулярна модель катодних променів стала завойовувати загальне визнання, хоча про природу електрики були найрізноманітніші судження. Так, німецький фізик Е.Віхерт вважав, що "електрика є щось уявне, існуюче реально тільки в думках ", а відомий англійський фізик лорд Кельвін у тому ж, 1897 році писав про електрику як про якусь "без перервної рідини ". 29 квітня1897 Томсон зробив своє знамените повідомлення на засіданні Лондонського королівського товариства. Ця подія стала підсумком багаторічної роботи Томсона і його співробітників. Ні Томсон, ні будь-хто інший ніколи не спостерігали електрон в буквальному сенсі, нікому не вдалося виділити окрему частинку з пучка катодних променів і виміряти її питома заряд. Автором відкриття є Дж. Дж. Томсона тому, що його уявлення про електрон були близькі до сучасним. У 1903 році він запропонував одну з перших моделей атома -"Пудинг з родзинками", а в 1904 припустив, що електрони в атомі розділяються на групи, утворюючи різні конфігурації, що обумовлюють періодичність хімічних елементів. Місце відкриття точно відомо - Кавендішської лабораторії (Кембрідж, Великобританія). Створена в 1870 році Дж. К. Максвелла, в наступні сто років вона стала"Колискою" цілого ланцюга блискучих відкриттів у різних галузях фізики, особливо в атомній і ядерній











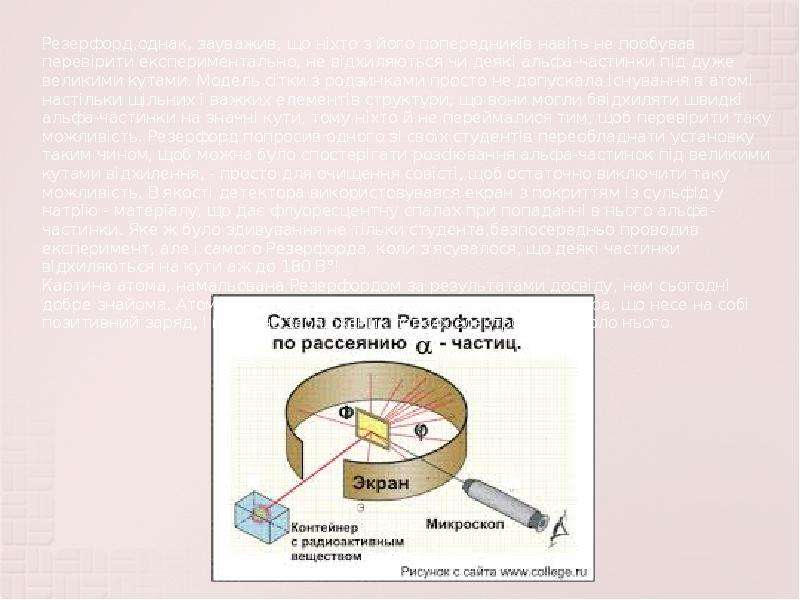

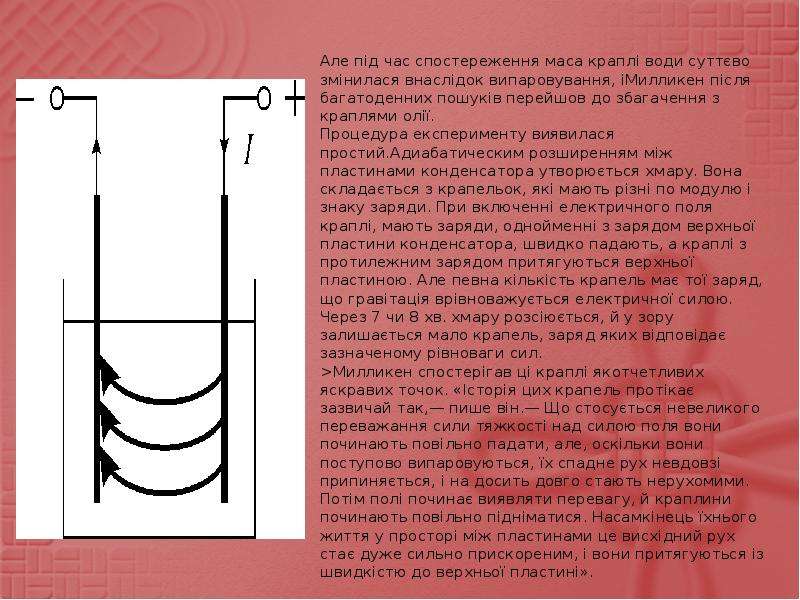





![Жидкость-жидкость. Эмульсии - грубодисперные системы из несмешивающихся жидкостей с размером капель от 100 до 5000 нм. Свойства эмульсии: 1. Эмульсии имеют поверхность раздела. 2. Эмульсии неустойчивы. 3. Эмульсии нуждаются в стабилизаторах [эмульгаторах]. Главным фактором устойчивости эмульсии – заряд [], или дзета-потенциал, образующийся при адсорбировании ионов стабилизатора на капельках эмульсии. Роль стабилизатора (эмульгатора): 1. Эмульгатор сообщает капелькам эмульсии заряд, за счёт диссоциации адсорбированных молекул. 2. Эмульгатор создаёт вокруг капелек эмульсии оболочку, препятствующую коалесценции (слипанию).](/documents/6c353d2abbf37f84da088e42c7fdf1ed/thumb.jpg)