Слайды и текст этой презентации
Слайд 1

Описание слайда:
Тема урока: «Карбонаты»
Цель урока: Изучить химические свойства солей угольной кислоты – карбонатов и гидрокарбонатов; приобрести навыки в решении экспериментальных и расчетных задач
Слайд 2

Описание слайда:
Тест – экспресс
1) Электронная конфигурация атома углерода?
2) Разновидности простого вещества, образованные одним и тем же химическим элементом?
3) Количество электронов на внешней электронной оболочке элементов IV группы главной подгруппы?
4) Летучие водородные соединения углерода и кремния?
5) Формула высших оксидов элементов IVа группы?
6) Масса 0,5 моль свинца?
7) Объем 2 моль метана при н.у.?
8) Чего больше по массе в угарном газе – кислорода или углерода?
9) Степень окисления углерода в угарном и углекислом газах?
10) Где больше атомов – в 1 литре угарного или в 1 литре углекислого газах?
Слайд 3

Описание слайда:
ОТВЕТЫ
1) Аллотропные видоизменения
2) 1s22s22p
3) Четыре
4) Метан СН4, силан SiH4
5) ЭО2
6) m=M.n; m=103,5г
7) V=Vm.n; V=44,8л
8) По массе больше кислорода
9) +2; +4
10) В 1л углекислого газа
Слайд 4

Описание слайда:
Фокус-покус для народа:
Стоит лишь подуть сквозь воду,
Как она легко-легко
Превратиться в молоко!
СО2 + Са(ОН)2 ↔ СаСО3 + Н2О
Слайд 5

Описание слайда:
Действие сильной кислоты может служить качественной реакцией на карбонаты:
СаСО3 + 2Н+ ↔ Са2+ + Н2О + СО2↑
Слайд 6

Описание слайда:
Как можно собрать СО2
М(воздуха)=29, т.е. СО2 тяжелее воздуха
Метод вытеснения воды невозможен из-за протекания реакции:
Метод вытеснения воздуха, т.к. М(СО2)=44;
CO2+H2O↔H2CO3
Слайд 7

Описание слайда:
Угольная кислота диссоциирует ступенчато:
1.H2CO3 ↔ Н+ + HCO3-
2. HCO3- ↔ Н+ + CO32-
Слайд 8
Описание слайда:
Соли угольной кислоты
↓ ↓
Нормальные Кислые
(карбонаты) (гидрокарбонаты)
Слайд 9
Описание слайда:
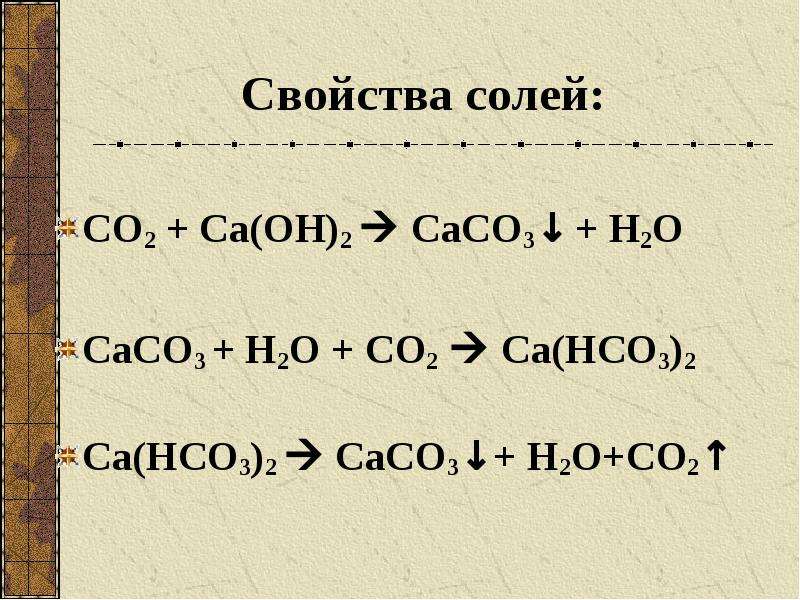
Свойства солей:
СО2 + Са(ОН)2 СаСО3↓ + Н2О
СаСО3 + Н2О + СО2 Са(НСО3)2
Са(НСО3)2 СаСО3↓+ Н2О+СО2↑
Слайд 10

Описание слайда:
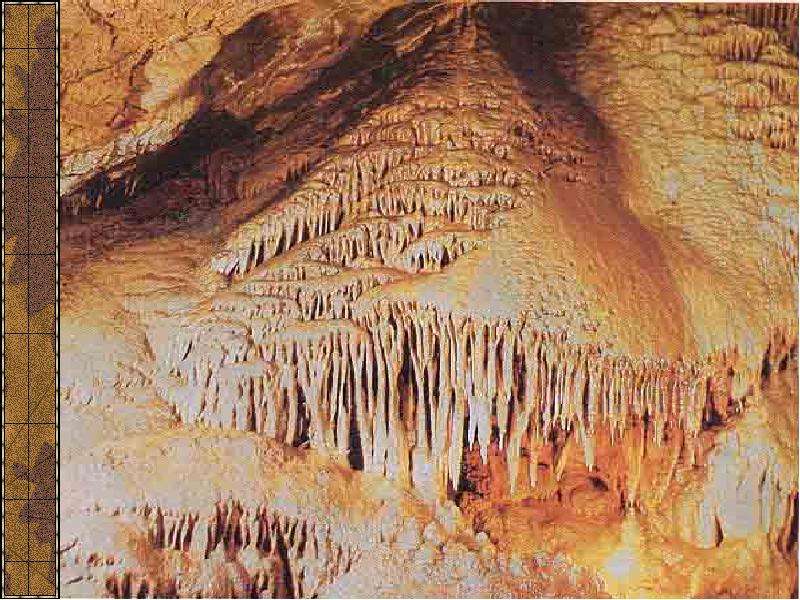
Пещера красная
Пещера красная
Слайд 11

Описание слайда:
Сталагмиты
Слайд 12

Описание слайда:
Сталактит «Пузатый»
Слайд 13

Описание слайда:
Сталактит «Огненный»
Слайд 14
Слайд 15

Слайд 16

Слайд 17

Описание слайда:
Изучением карстовых пещер занимается наука – спелеология
Слайд 18

Описание слайда:
Соли угольной кислоты:
Мрамор, известняк, мел – СаСО3
На земле живут три брата
Из семейства Карбонатов.
Старший брат – красавец Мрамор,
Славен именем Карары,
Превосходный зодчий. Он
Строил Рим и Парфенон.
Слайд 19

Описание слайда:
Доломит CaCO3. MgCO3 – обычно содержит глины и известняки, применяется для получения извести, солей магния, как удобрение(доломитовая мука).
Доломит CaCO3. MgCO3 – обычно содержит глины и известняки, применяется для получения извести, солей магния, как удобрение(доломитовая мука).
Малахит Cu2(ОН)2CO3 – хрупкий, цвет ярко-зеленый, темно-зеленый, блестит. Из него изготовляют художественно-декоративные предметы,используют для получения меди.
Слайд 20

Описание слайда:
Сидерит FeCO3 – минерал бурого цвета, служит рудой для получения железа.
Кальцинированная сода Na2CO3 – белый порошок, используется в производстве стекла, мыла, бумаги, моющих средств.
Питьевая сода NaHCO3 – белый порошок, плохо растворяется в воде, используют в медицине, в пищевой промышленности, как средство огнетушения.
Слайд 21

Описание слайда:
Презентация разработки темы в курсе
9 класса.
Подготовила учитель химии
ОГРИНА
СВЕТЛАНА ЮРЬЕВНА
Слайд 22
Описание слайда:
Помогите различить суспензию мела и суспензию гашеной извести
Презентацию на
тему Карбонаты можно скачать бесплатно ниже: