Слайды и текст этой презентации
Слайд 1

Описание слайда:
Тема: Серная кислота, свойства серной кислоты.
Слайд 2

Описание слайда:
Состав
Кислоты - это сложные вещества, в молекулах которых содержат атомы водорода и кислотный остаток
H-R, где R-кислотный остаток
При электролитической диссоциации кислот в водном растворе образуются катионы водорода и анион кислотного остатка
Слайд 3

Описание слайда:
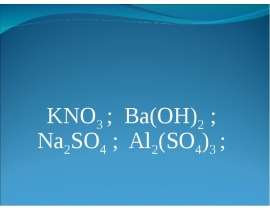
Классификация кислот
Одноосновные кислоты, например, HCl, HNO3 (отщепляют при диссоциации один атом водорода)
Многоосновные кислоты, например, H2SO4, H3PO4 (отщепляют при диссоциации несколько атомов водорода)
Слайд 4
Описание слайда:
Разбавление серной кислоты
Относительно смешивания серной кислоты с водой с давних пор существует строгое правило: «Сначала вода, потом кислота, иначе произойдет ужасное».
Если же сделать наоборот, то первые же порции воды, оставшись наверху (вода легче кислоты) и взаимодействуя с кислотой, разогреваются так сильно, что вскипают и разбрызгиваются вместе с кислотой; могут попасть в глаза, на лицо и одежду.
Слайд 5
Описание слайда:
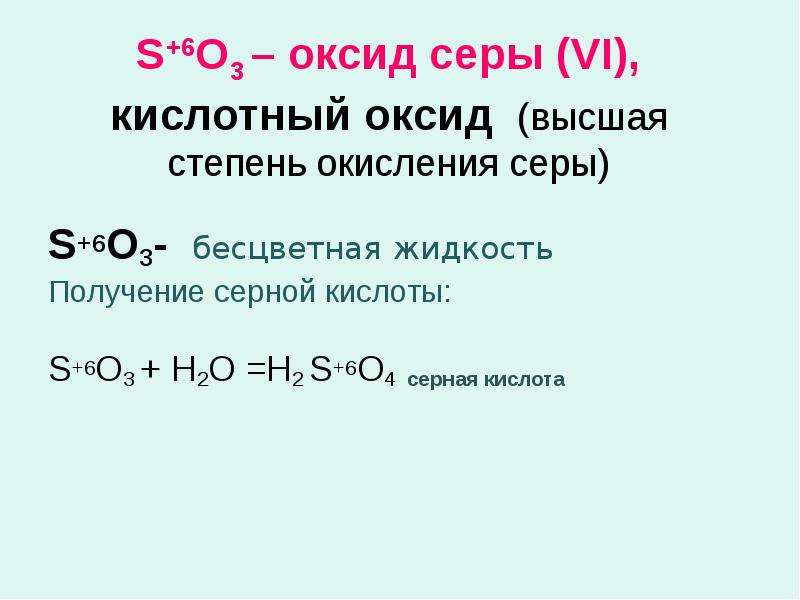
S+6O3 – оксид серы (VI), кислотный оксид (высшая степень окисления серы)
S+6O3- бесцветная жидкость
Получение серной кислоты:
S+6O3 + Н2О =Н2 S+6O4 серная кислота
Слайд 6

Описание слайда:
Химические свойства серной кислоты
разбавленная серная кислота проявляет все характерные свойства кислот:
С оксидами металлов.(реакция обмена)
Н2SO4+MeO→MeSO4+H2O
2. С основаниями.(реакция обмена, реакция нейтрализации)
Н2SO4+Me(OН)n→MeSO4+H2O
3. С металлами.
Н2SO4+Me(до Н)→MeSO4(р)+H2↑(реакция замещения)
4.С солями( реакция обмена)
Н2SO4+MeR(Р)→MeSO4 (Р)+HR
(протекает в том случае, если образуется осадок или газ)
Слайд 7

Описание слайда:
Качественная реакция на ион –SO42-
Качественная реакция на ион –SO42-
Реактивом на серную кислоту и ее соли является катион бария , т.к. с ионами бария сульфат ион образует белый нерастворимый сульфат бария, выпадающий в осадок.
Ва2++SO42- = BaSO4↓
Слайд 8

Описание слайда:
Концентрированная серная кислота
Ме+Н2SO4(кoнц)→МеSO4+H2O+(Н2S,S,SO2)
Серная кислота(конц) восстанавливается до
(Н2S,S,SO2) в зависимости от активности металла и условий протекания реакции.
Железо и алюминий пассивируются кислотой, т.е покрываются защитной пленкой, поэтому кислоту(конц) можно перевозить в стальных и алюминиевых цистернах.
Сu+2H2SO4(конц)→CuSO4+2H2O+SO2
4Zn+5H2SO4(конц)→4ZnSO4+4H2O+H2S
Концентрированная серная кислота способна отнимать воду из молекул органических веществ, обугливая их.
Взаимодействие кислоты с сахарозой(C12H22O11)
C12H22O11 + 2H2SO4(конц) = 11C + 13H2O↑ +2SO2↑ +CO2↑
Слайд 9
Слайд 10

Слайд 11

Слайд 12

Слайд 13

Презентацию на
тему Серная кислота, свойства серной кислоты можно скачать бесплатно ниже: