Слайды и текст этой презентации
Слайд 1

Описание слайда:
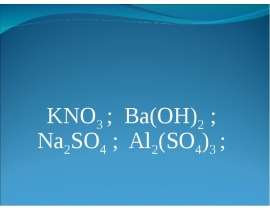
Электролитическая диссоциация
Слайд 2

Слайд 3

Описание слайда:
Процесс распада электролита на ионы называется электролитической диссоциацией.
Слайд 4
Описание слайда:
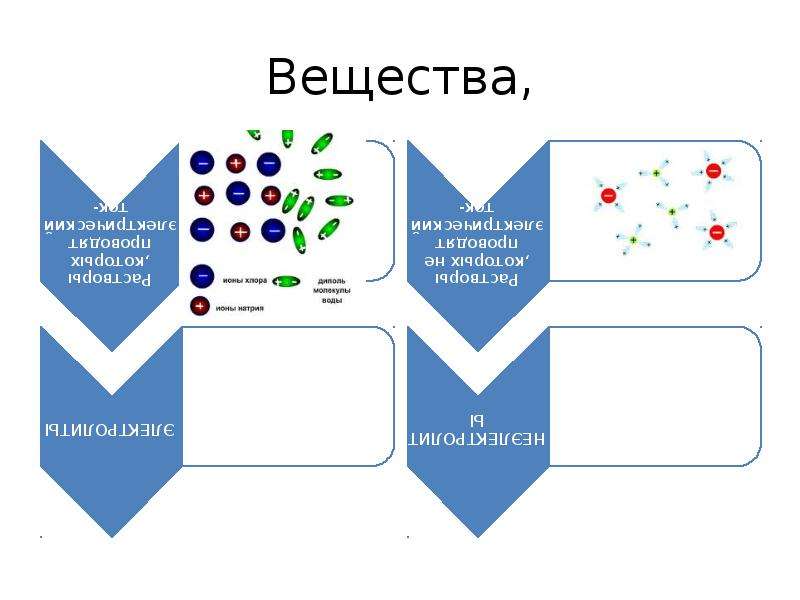
Вещества,
Слайд 5
Описание слайда:
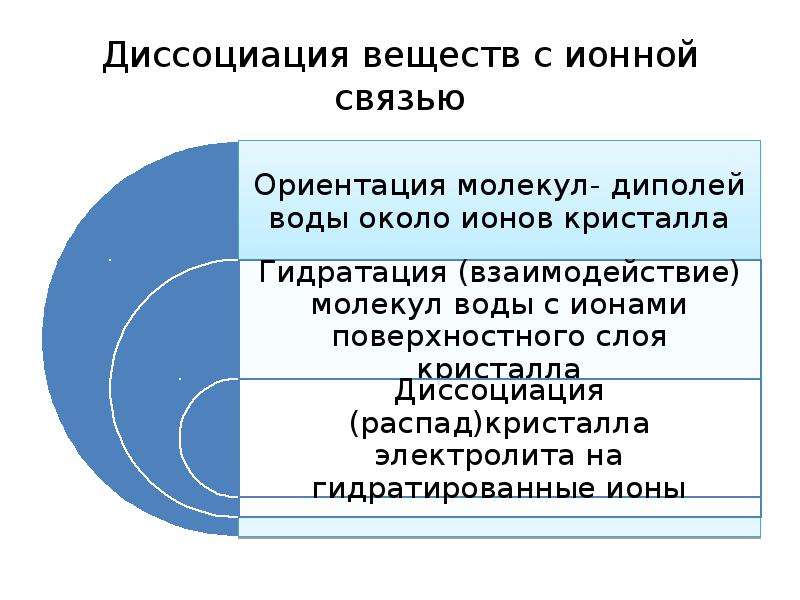
Диссоциация веществ с ионной связью
Слайд 6
Описание слайда:
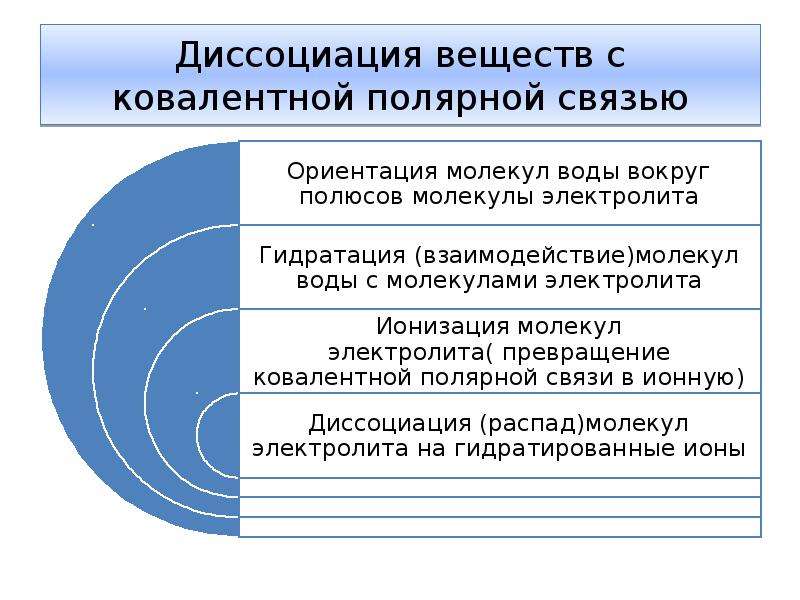
Диссоциация веществ с ковалентной полярной связью
Слайд 7
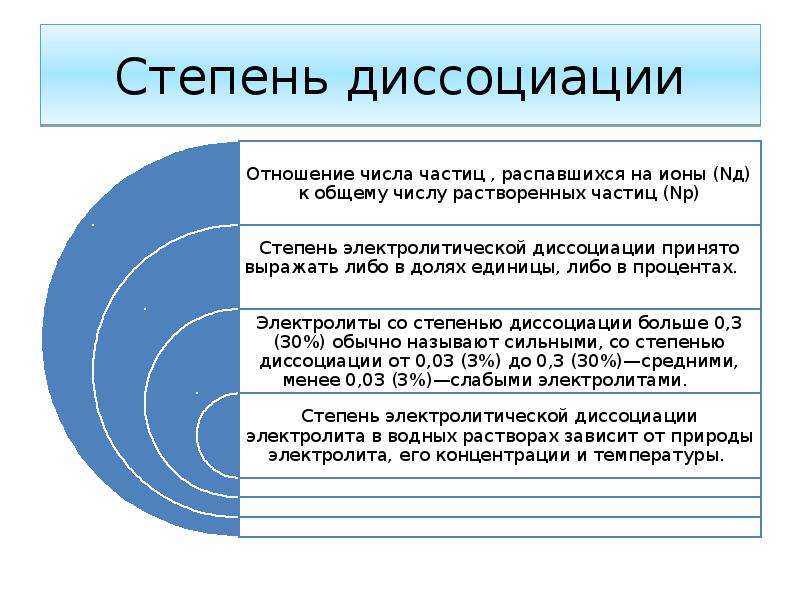
Описание слайда:
Степень диссоциации
Слайд 8

Описание слайда:
Электролиты условно делятся:
Сильные электролиты диссоциируют практически полностью (α = 1).
Слайд 9

Описание слайда:
К сильным электролитам относятся
Слайд 10

Описание слайда:
К слабым электролитам относятся:
1) неорганические кислоты (H2CO3, H2S, HNO2, H2SO3 , HCN, H3PO4, H2SiO3, HCNS, HСlO и др.);
2) вода (H2O);
3) гидроксид аммония (NH4OH);
4) большинство органических кислот
(например, уксусная CH3COOH, муравьиная HCOOH);
5) нерастворимые и малорастворимые соли и гидроксиды некоторых металлов
Слайд 11

Описание слайда:
Тест по теме "Электролитическая диссоциация. Реакции ионного обмена"
1. К неэлектролитам относится:
1) нитрат калия 2) гидроксид бария 3) хлорид кальция 4) оксид азота(II)
2. К хорошо растворимым электролитам относится:
1) бромид натрия 2) гидроксид цинка 3) карбонат кальция 4) гидроксид магния
3. В водном растворе наибольшее количество сульфат-анионов образуется при
диссоциации 1 моль:
1) Al2(SO4)3 2)PbS 3) CaSO4 4) K2SO4
Слайд 12

Описание слайда:
Тест по теме "Электролитическая диссоциация
4. Катионы металла и анионы кислотного остатка образуютя при диссоциации:
1) оксидов 2) кислот 3) солей 4) оснований
5. Выберите верную запись правой части уравнения диссоциации карбоната калия:
1) = K+ + CO3¯ 2) = K+ + CO32- 3) = 2K+ + CO32- 4) = 2K+ + HCO3¯
6. Наибольшее количество анионов образуется при диссоциации 1 моль:
1) AlCl3 2) Zn(OH)2 3) Al(OH)3 4) Zn(NO3)2
Слайд 13

Описание слайда:
Использованные материалы:
Презентацию на
тему Электролитическая диссоциация (8 класс) можно скачать бесплатно ниже: